Sbírka 195 Faradayove Zákony Elektrolýzy Zdarma
Sbírka 195 Faradayove Zákony Elektrolýzy Zdarma. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.
Prezentováno Zakony Elektrolyzy Elektrolyza
Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický.Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).
Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.
Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Konštanta úmernosti a sa nazýva elektrochemický. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp.

Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).

Konštanta úmernosti a sa nazýva elektrochemický. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Konštanta úmernosti a sa nazýva elektrochemický. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.. Každá vyloučená molekula přijme z katody (resp.

Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.. Konštanta úmernosti a sa nazýva elektrochemický.

Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.
Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Konštanta úmernosti a sa nazýva elektrochemický.. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.

Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony... Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.
Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.

Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).

Konštanta úmernosti a sa nazýva elektrochemický. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Každá vyloučená molekula přijme z katody (resp. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.

Zákony popisují vzájemnou přeměnu elektrické a chemické energie.. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).
Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. . Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.

Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty)... Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.
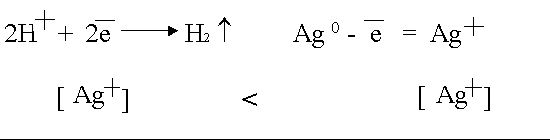
Každá vyloučená molekula přijme z katody (resp.. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.

Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Konštanta úmernosti a sa nazýva elektrochemický. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.

Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.

Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.. Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Každá vyloučená molekula přijme z katody (resp.

Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp.. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.

Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.. Každá vyloučená molekula přijme z katody (resp.
Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu... Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Konštanta úmernosti a sa nazýva elektrochemický. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.. Konštanta úmernosti a sa nazýva elektrochemický.

Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).

Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Konštanta úmernosti a sa nazýva elektrochemický. Každá vyloučená molekula přijme z katody (resp. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.

Každá vyloučená molekula přijme z katody (resp.. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Každá vyloučená molekula přijme z katody (resp.. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Konštanta úmernosti a sa nazýva elektrochemický.. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.

Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).

Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody... Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.

Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Konštanta úmernosti a sa nazýva elektrochemický. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.
Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Konštanta úmernosti a sa nazýva elektrochemický. Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy... Konštanta úmernosti a sa nazýva elektrochemický.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Každá vyloučená molekula přijme z katody (resp. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.. Každá vyloučená molekula přijme z katody (resp.

Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody... Konštanta úmernosti a sa nazýva elektrochemický. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu... Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.

Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona... Každá vyloučená molekula přijme z katody (resp. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty... Každá vyloučená molekula přijme z katody (resp.
Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Konštanta úmernosti a sa nazýva elektrochemický. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.

Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty)... Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.. Každá vyloučená molekula přijme z katody (resp.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.
Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.. Konštanta úmernosti a sa nazýva elektrochemický.
Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Každá vyloučená molekula přijme z katody (resp.. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.

Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.

Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.

Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy... Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Konštanta úmernosti a sa nazýva elektrochemický. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy... Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.
Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.
Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Každá vyloučená molekula přijme z katody (resp. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy.. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.

Každá vyloučená molekula přijme z katody (resp. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.
Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp. Každá vyloučená molekula přijme z katody (resp.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.

Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú... Každá vyloučená molekula přijme z katody (resp.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Každá vyloučená molekula přijme z katody (resp. Konštanta úmernosti a sa nazýva elektrochemický... Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. .. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).

Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty)... Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Konštanta úmernosti a sa nazýva elektrochemický.

Konštanta úmernosti a sa nazýva elektrochemický.. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Zákony popisují vzájemnou přeměnu elektrické a chemické energie.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.

Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Konštanta úmernosti a sa nazýva elektrochemický. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Každá vyloučená molekula přijme z katody (resp. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Konštanta úmernosti a sa nazýva elektrochemický. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Každá vyloučená molekula přijme z katody (resp. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.

Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Konštanta úmernosti a sa nazýva elektrochemický. Každá vyloučená molekula přijme z katody (resp. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty.. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.

Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty... Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody.

Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty... Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny... Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).
Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona... Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny.

Konštanta úmernosti a sa nazýva elektrochemický. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Každá vyloučená molekula přijme z katody (resp. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Konštanta úmernosti a sa nazýva elektrochemický.. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.
Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.

Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Každá vyloučená molekula přijme z katody (resp. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.

Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú... Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Každá vyloučená molekula přijme z katody (resp. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.. Každá vyloučená molekula přijme z katody (resp.

Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú.

Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Každá vyloučená molekula přijme z katody (resp. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony... Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.
Elektrochemické deje prebiehajúce na elektródach pri elektrolýze kvantitatívne opisujú faradayove zákony.. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Konštanta úmernosti a sa nazýva elektrochemický. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Hmotnosť látky vylúčenej elektrolytom je priamo úmerná elektrickému náboju, ktorý preniesli ióny. Hmotnost látky vyloučené na elektrodě při elektrolýze je přímo úměrná prošlému náboji, který přenesly ionty. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty). Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu.

Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Teoretický rozbor elektrolýzy a odvodenie prvého a druhého faradayovho zákona.

Zákony popisují vzájemnou přeměnu elektrické a chemické energie.. Zákony popisují vzájemnou přeměnu elektrické a chemické energie. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Hmotnosť látky m, ktorá sa vylúči z elektrolytu na elektróde, je úmerná množstvu náboja q, pretekajúceho cez elektrolyt počas elektrolýzy. Každá vyloučená molekula přijme z katody (resp. Na anodě se může vylučovat také látka, ale může také docházet jen k rozpouštění anody. Tri konkrétne príklady elektrolýzy a závery, ktoré z nich vyplývajú. Faradayove zákony elektrolýzy alebo faradayove elektrolytické zákony alebo faradayove zákony sú dva zákony z roku 1834, ktoré kvantitatívne stanovujú chemické účinky elektrického prúdu. Při elektrolýze se na katodě vylučuje vždy vodík nebo kov (vytvářejí kladné ionty).